Autor: Przemysław Borowy,
Klinika Reumatologii i Immunologii Szpital Specjalistyczny im. J. Dietla w Krakowie
Mimo ewolucji definicji osteoporozy i przeniesienia akcentów na ryzyko złamania, badanie densytometryczne pozostaje podstawowym narzędziem do oceny gęstości mineralnej kości (Bone Mineral Density -BMD). Densytometria za pomocą podwójnej absorbcjometrii rentgenowskiej (DXA - Dual Energy X-ray Absorptiometry) jest jedyną rekomendowaną techniką wykorzystywaną w praktyce klinicznej do diagnozowania OP. Nie mierzy ona jednak rzeczywistej gęstości kości, mikro i makrostruktury decydujących o jakości kości. Tych informacji dostarczają: ilościowa tomografia komputerowa (quantitive computer tomography – QCT), rezonans magnetyczny, badanie ultrasonograficzne (quantitative ultrasound - QUS), czy Trabecular Bone Score – TBS. Wszystkie one mają jednak ograniczone zastosowanie: w badaniach klinicznych, ocenie złamań i prognozowaniu ryzyka kolejnych, a także w diagnostyce różnicowej chorób metabolicznych kości. Osobne miejsce w diagnostyce zajmuje R.E.M.S – technika ultrasonograficzna, która przeszła walidacje w wielu krajach i jest narzędziem skryninigowym w diagnostyce osteoporozy. W Polsce jest to narzędzie pomocnicze, jako tanie, bezpieczne, bo pozbawione promieniowania rentgenowskiego narzędzie przesiewowe dla dorosłych ale tez dzieci i kobiet w ciąży[1].
Od 1994r WHO kryteria rozpoznania osteoporozy oparto na badaniu DXA wyróżniając następujące kategorie diagnostyczne (tabela 1)[2],[3].
Tabela. 1. Kryteria diagnostyczne WHO: wartość wskaźnika T lub Z score.
norma (+ 1.0 )- (- 1.0)
osteopenia - 1.0 - -2.4
osteoporoza ≤ - 2.5
Wskaźnik T score jest liczbą odchyleń standardowych (SD) od wzorcowej, szczytowej masy kostnej osób w wieku 20-29 lat, tej samej płci w referencyjnej bazie danych (NHANES III). Wartości Z score odnoszą się do osób tej samej płci w wieku pacjenta. Chorobę rozpoznajemy na podstawie niższej wartości Tscore w jednym z dwóch rekomendowanych miejsc pomiaru. Wg WHO jest to odcinek lędźwiowy kręgosłupa i bliższy koniec kości udowej. Badanie przedramienia ma warunkowe zastosowanie tylko w przypadku nadczynności przytarczyc, niemożności wykonania lub interpretacji centralnej DXA lub z powodu otyłości przekraczającej dopuszczalny ciężar dla aparatów DXA. Każda z lokalizacji dostarcza innych informacji, co wynika z różnej budowy kości (ilość kości korowej i beleczkowej, inna architektonika beleczek kostnych, różna szczytowa masa kostna, inny obrót kostny). Tradycyjne podejście by wykonywać tylko DXA kręgosłupa u chorych przed 65 r życia zostało zarzucone. W diagnostyce OP rekomendowane jest badanie w obu miejscach pomiaru. W wybranych sytuacjach klinicznych zalecane jest obustronne badanie kości udowej.
Powtarzalność badań densytometrycznych jest niska. Różnice miedzy kolejnymi pomiarami mogą sięgać kilku procent. Wynika to z metodologii badania, rozdzielczości aparatu, pozycjonowania pacjenta, dlatego zalecane jest wyznaczenie błędu pracowni dla każdego technika i wyliczenie minimalnej istotnej zmiany (LSC). Wartość LSC pozwala wnioskować, czy zmiana w kolejnych badaniach u pacjenta jest istotna statystycznie, a nie wynika z błędu pomiaru. Mimo tych ograniczeń DXA może być wykorzystywana do monitorowania leczenia. W tym wskazaniu minimalny odstęp miedzy badaniami powinien wynosić rok. DXA to również precyzyjne narządzie obrazowania trzonów kręgów w celu wykrycia złamań kompresyjnych[4]. Boczne badanie kręgosłupa (vertebral fracture assesment VFA) z prawie 100% swoistością w stosunku do rentgena rozpoznaje średnie i ciężkie złamania kręgów wg klasyfikacji Genanata.
DXA kręgosłupa.
Trzony kręgów zbudowane są w 80% z kości beleczkowej. Kość beleczkowa ma wielokrotnie szybszy obrót kostny (2-5% rocznie), niż kość korowa. Również procesy kościotworzenia – mineralizacja w trakcie leczenia anabolicznego lub antyresorbcyjnego - może być obserwowana już po 6-12 miesiącach. DXA Kręgosłupa jest przydatna w wczesnej diagnostyce OP pomenopauzalnej, wtórnych osteoporozach z dużym obrotem kostnym i oceny skuteczności terapii. Jednak aktywna przebudowa kośćca, wymuszona funkcją podporową szkieletu osiowego, prowadzi równocześnie do zmian zwyrodnieniowych. W efekcie zmiany te zniekształcają wynik DXA, najczęściej go zawyżając. Również złamania kompresyjne – najczęstsze w OP – zmieniają wartość BMD. Osteomalacja, uwarunkowana niedoborem witaminy D3, zaniża BMD.
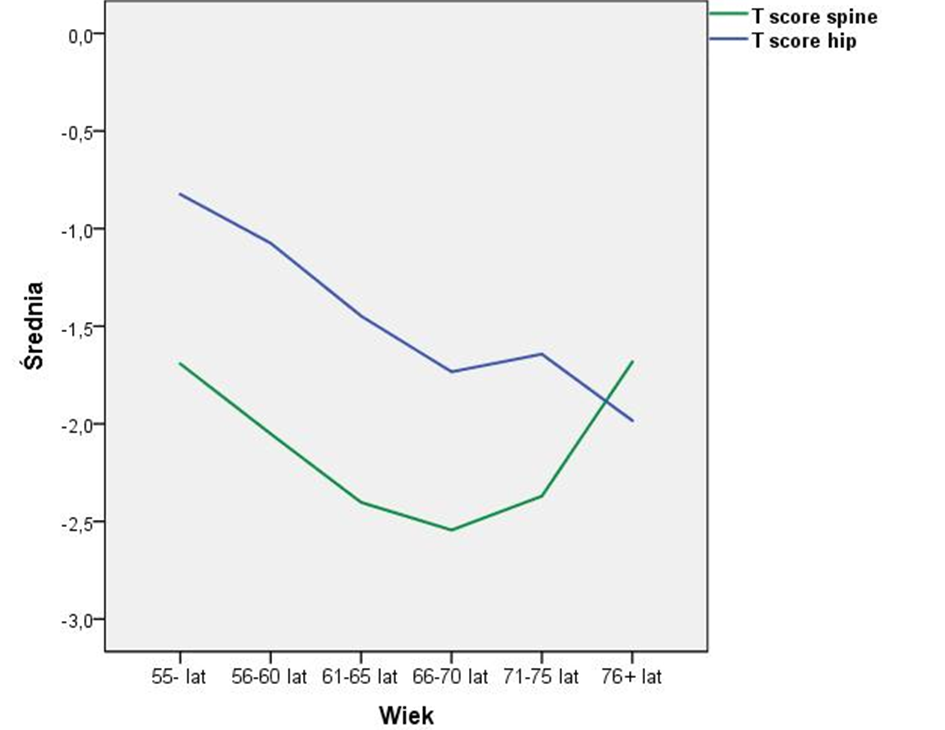
Rys 1. Rozkład wskaźnika T score kręgosłupa i T score dla neck w zależności od wieku w losowo wybranej populacji 6500 kobiet z Małopolski. ( praca doktorska autora)
Pomiar BMD dokonuje się w zakres kręgów L1-L4. Z analizy należy wykluczyć kręgi z artefaktami, zmianami zwyrodnieniowymi, złamaniami, cementem kostnym, przebudowane nowotworowo. Oceniając poprawność badania sprawdzamy, czy pola powierzchni i badana gęstość (bone mineral consent -BMC) rosną od L1 do L4. Finalnie wartość T lub Z score nie powinna różnić się więcej niż 1 SD miedzy poszczególnymi kręgami. W przypadku opisanych odchyleń z analizy można wykluczyć nieprawidłowe kręgi, a analizie poddać pozostałe. Muszą to być jednak minimum dwa sąsiednie kręgi. Nigdy nie powinno się analizować pojedynczego kręgu. U pacjentów z wadami postawy, widoczna na wydruku skolioza powinna być skomentowana przez technika jako trwałe zaburzenie postawy. Ma to wykluczyć przypadkowe nieprawidłowe ułożenie pacjenta. Wszystkie te ograniczenia sprawiają, że u niektórych pacjentów ze złamaniami kompresyjnym w odcinku lędźwiowym kręgosłupa, BMD jest często wyższe niż -2,5SD. Powoduje to błędy w rozpoznaniu choroby ( jej niedoszacowanie) i jest jednym z powodów zmiany definicji OP. Trzeba jednak podkreślić, że prawidłowo wykonana densytometria kręgosłupa pozostaje najlepszym narzędziem do ceny ryzyka złamania kręgosłupa i pozostałych złamań osteoporotycznych.
DXA bliższego końca kości udowej (bkku) – odrębności badania, wartość w ocenie ryzyka złamania.
W zakresie biodra ocenia się BMD dla jego najwęższego fragmentu ( neck) oraz total ( będącego sumą pomiarów z wszystkich analizowanych elementów kości udowej). Wartość najniższa jest decydująca dla rozpoznania. Pomiar w obrębie trójkąta Warda jest nieprzydatny i w nowych aparatach nie jest już wykonywany. Zaletą DXA kości udowej jest powtarzalność badania, ponieważ neck rzadko podlega zmianom zwyrodnieniowym. Jednak korowa budowa kości udowej opóźnia pojawienie się zmian osteoporotycznych[5]. Wolniej też odpowiada na leczenie (poprawa widoczna jest często drugim i kolejnych latach leczenia). Kontrolne badanie DXA zaleca się wykonywać po 3-5 latach w zależności od sytuacji klinicznej[6]. Klinicyści podkreślają jednak rolę badania DXA jako czynnika motywującego, poprawiającego persistence terapii. W zaawansowanych zmianach zwyrodnieniowych kręgosłupa i stawów biodrowych pojawiają się trudności dotyczące prawidłowego pozycjonowania kończyn, co wpływa na wynik w przypadku monitorowania leczenia. Oceniając ustawienie kości udowej należy sprawdzić, czy krętarz mniejszy jest niewidoczny lub prawie niewidoczny, a długa oś kości udowej jest równoległa do osi kręgosłupa. Widoczne na wydruku odchylenia powinny zostać skomentowane przez technika jako niemożliwe do skorygowania przy prawidłowym ułożeniu pacjentki. Pomiar DXA w zakresie biodra jest jedynym miejscem uwzględnionym w kalkulatorze ryzyka złamania FRAX, ponieważ najlepiej prognozuje ryzyko złamania biodra[7]. Jego najnowsza wersja: FRAX Plus uwzględnia jednak wynik z DXA kręgosłupa.
Badanie rentgenowskie.
Badanie rentgenowskie służy rozpoznawaniu złamań. Jego wykorzystanie nie budzi wątpliwości w przypadku złamań obwodowych. Złamanie kompresyjne, zgodnie z wytycznymi National Osteoporosis Foundation (NOF) z 2013 „jest potwierdzeniem osteoporozy nawet bez wyniku DXA”[8], dlatego jednoznaczne rozpoznanie go ma ogromne znaczenie. Do jego weryfikacji służą półilościowe kryteria zaproponowane przez Genanta[9]. Zgodnie z nimi obniżenie wysokości trzonu kręgu lub jego części o 20% lub więcej jest potwierdzeniem złamania. Stopień złamania określa się w 3 stopniowej skali. Prezentuje je tabela nr 1.
Tabela 1. Klasyfikacja złamań kompresyjnych wg Genanta.
|
Typ złamania w zależności od lokalizacji |
|||
|
Stopień złamania |
Tylna |
Środkowa |
Przednia/całkowita |
|
łagodne 20-25% |
Klinowe |
dwuwklesłe |
zmiażdżeniowe |
|
Umiarkowane 26-40% |
|||
|
ciężkie > 40% |
|||
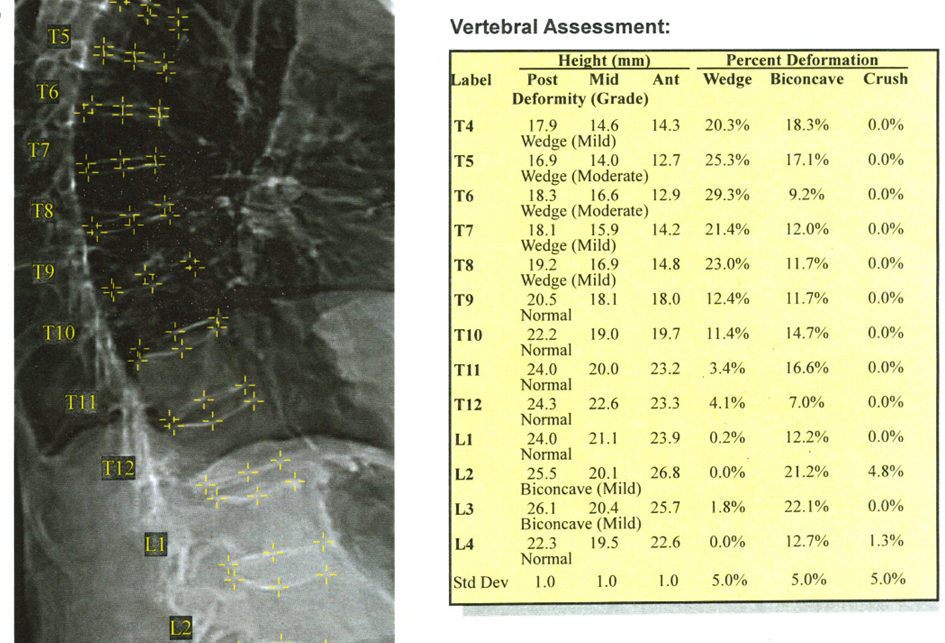
Alternatywną metodą oceny złamań jest morfometria absorbcjometryczna. To rodzaj densytometrii przeznaczonym do diagnostyki złamań kręgów od Th4 do L4. Badanie można wykonać każdym aparatem DXA, analizując kształt i 6 punktową ocenę boczną kręgów ( rysunek 2). W tym przypadku nie przeprowadza się analizy gęstości mineralnej, a jedynie mierzy się wysokości kręgów. Porównując je między sobą lub wysokości przedniej, środkowej i tylnej powierzchni trzonu ocenia się je zgodnie z kryteriami Genanta, klasyfikując złamanie w 3 stopniowej skali. Ten typ badania densytometrycznego, określany jako VFA (Vertebral fracture assessment) wymaga mniejszych dawek promieniowania rentgenowskiego, niż klasyczne badanie rentgenowskie. Niestety, rozdzielczość DXA nie pozwala precyzyjnie wykrywać małych deformacji (obniżenia wysokości <25%)[10]. Ponieważ złamania kręgosłupa są najczęstsze w osteoporozie, a prawie 70% z nich jest bezobjawowa, morfometria jest przydatnym narzędziem skryningowym[11].
Rysunek 2. Morfometria kręgosłupa z pomocą DXA. Algorytm analizuje 6 punktów każdego kręgu, obliczając poszczególne wymiary i porównując je ze sobą i sąsiednim kręgiem.
Trabecular Bone Score (TBS) – sposób na niediagnostyczny wynik DXA.
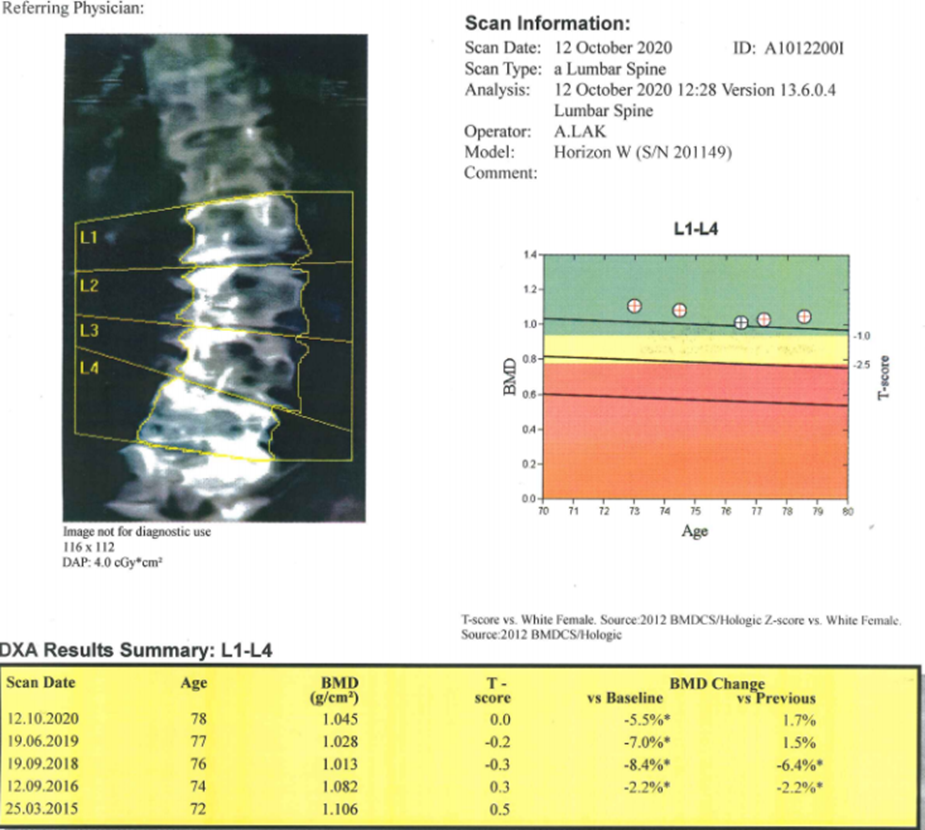
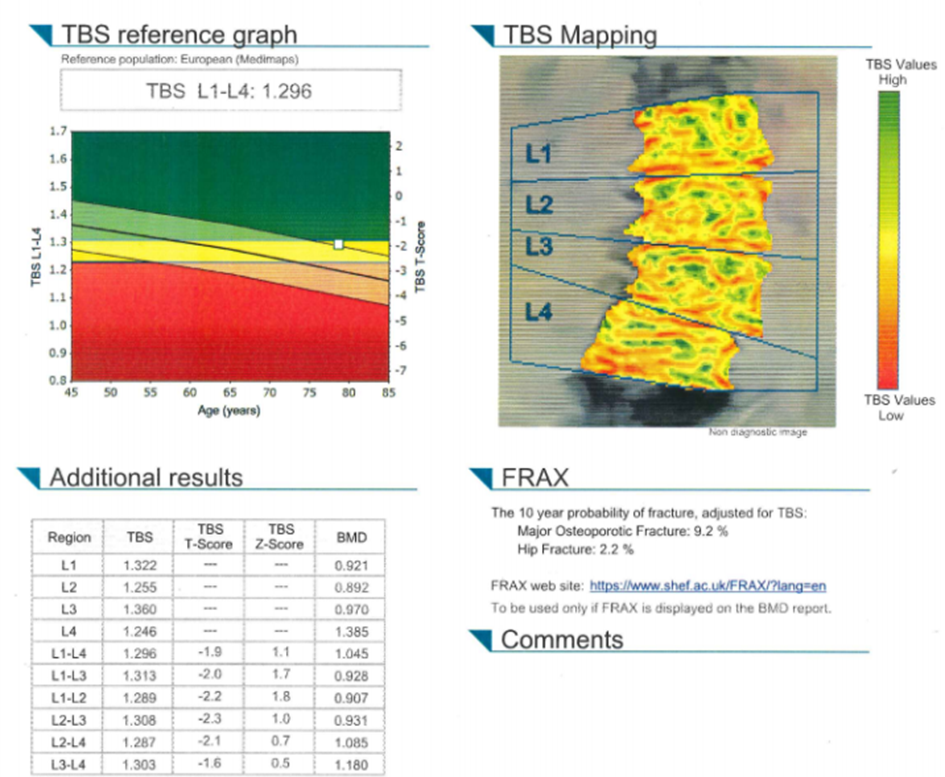
W przypadku choroby zwyrodnieniowej, wad postawy, patologicznych zmian i artefaktów przed i za obszarem badania DXA - rzeczywista gęstość mineralna kości może odbiegać od wyniku badania (tabela 3). Zmiany najczęściej zawyżają wartość BMD, sprawiając, że część chorych nie spełnia kryteriów diagnostycznych mimo ewidentnej choroby. Naczyniaki, wrodzone deformacje, przerzuty osteolityczne mogą zaniżać wynik DXA. Często u jednego pacjenta występuje kilka zmian dyskwalifikujących DXA kręgosłupa z diagnostyki. TBS opiera się na analizie tekstury gęstości optycznej 2D zwykłego obrazu densytometrycznego, który jest rzutem 3D struktury kości[12]. Gęsta struktura kości generuje duża liczbę pikseli, a niska gęstość mineralna – małą liczbę pikseli. Algorytm przelicza i porównuje otrzymane wyniki do wartości referencyjnych. Wyniki jest niezależny od zmian zwyrodnieniowych i innych patologii. Pozwala lepiej prognozować ryzyko złamania niż DXA (predykcja złamania TBS + DXA jest wyższa niż samo DXA o 25%). FRAX z użyciem TBS jest czulszy i kwalifikuje do leczenia ok 25% więcej pacjentów[13]. W praktyce TBS pomaga w podejmowaniu decyzji terapeutycznych w chorobach prowadzących do złamań z DXA >-2,5 Tscore (cukrzyca, POCHP, RZS, przewlekłej chorobie nerek, nadczynności przytarczyc). Przykład rozbieżności miedzy badaniami pokazuje rysunek 4.
Tabela 3. Potencjalne zaburzenia wpływające na wynik badania densytometrycznego kręgosłupa.
|
Rodzaj zaburzeń |
Lokalizacja |
||
|
Za kręgosłupem |
W obrębie kręgu |
Przed kręgosłupem |
|
|
Choroba zwyrodnieniowa kręgosłupa |
X |
X |
X |
|
Spondyloartropatia i zmiany zapalne |
X |
X |
X |
|
Miażdzyca |
X |
||
|
Skolioza I pochodne |
X |
||
|
Ciało obce |
X |
X |
|
|
Kontrast medyczny |
X |
X |
|
|
Zmiany w obrębie jelit |
X |
||
|
Artefakty |
X |
X |
X |
|
Naczyniaki, nowotwory złośliwe i przerzuty |
X |
||
Rysunek 4. Wynik badania DXA i TBS u 78 letniej pacjentki ze złamaniami kompresyjnymi (ze źródeł własnych autora).
FRAX, FRAX Plus, GARWAN i inne kalkulatory ryzyka złamania.
Kalkulatory ryzyka złamania jak FRAX i FRAX plus stanową uzupełnienie diagnostyki OP o czynniki ryzyka. Pozwalają prognozować 10-letnie ryzyko złamania i są pełnoprawnym narzędziem do rozpoznawania rozpoczęcia terapii[14]. Dostępne wersje online, są łatwe, szybkie i zwalidowane w populacji polskiej i mogą być wykorzystywane w codziennej praktyce lekarskiej w sytuacjach wątpliwych i przed rozpoczęciem leczenia.
[1] Jeka S. Diagnostyka obrazowa chorób reumatologicznych i monitorowania leczenia biologicznego. Tom3. Via Medica.2022.
[2] World Health Organization: Assessment of fracture risk and its application to screening for postmenopausal osteoporosis. Technical Report Series 843, Geneva 1994
[3] Kanis JA on behalf of the World Health Organization Scientific Group (2008) Assessment of osteoporosis at the primary health-care level. Technical Report. WHO Collaborating Centre, University of Sheffield, UK
[4] Lee JH, Lee YK, Oh SH, Ahn J, Lee YE, Pyo JH, Choi YY, Kim D, Bae SC, Sung YK, Kim DY (2016) A systematic review of diagnostic accuracy of vertebral fracture assessment (VFA) in postmenopausal women and elderly men. Osteoporos Int 27:1691–1699
[5] Black GM, Wahner HW, Fogelman I: The evaluation of osteoporosis: Dual Energy X-ray Absorptiometry and Ultrasound in Clinical Practice. Martin Dunitz Ltd, London 1999
[6] Shoback D, Rosen CJ, Black DM, Cheung AM, Murad MH, Eastell R. Pharmacological Management of Osteoporosis in Postmenopausal Women: An Endocrine Society Guideline Update. J Clin Endocrinol Metab. 2020 Mar 1;105(3).
[7] Leib ES, Lewiecki EM, Binkley N, Hamdy RC. International Society for Clinical Densitometry. Official positions of the International Society for Clinical Densitometry. J Clin Densitom. 2004; Spring;7(1):1-6
[8] Cosman F, de Beur SJ, LeBoff MS, Lewiecki EM, Tanner B, Randall S, Lindsay R. Clinician’s guide to prevention and treatment of osteoporosis. Osteoporos Int 2014;25:2359-81
[9] Genant HK, Wu CY, Van Kuijk C, Nevitt M. Vertebral fracture assessment using a SQ technique. J Bone Miner Res 1993;8:1137-48
[10] Gallacher,S.J.; Gallagher,A.P.; McQuillian,C.; Mitchell,P.J.; Dixon,T.The prevalence of vertebral fracture amongst patients presenting with non-vertebral fracturesAuthors: Osteoporos.Int., 2007, 18, 2, 185-192
[11] Lyles KW, Gold DT, Shipp KM, Pieper CF, Martinez S, Mulhausen PL. Association of osteoporotic vertebral compression fractures with impaired functional status. Am J Med 1993; 94(6):595-601 ].
[12] Warzecha M. et all. Trabecular Bone Score (TBS) w praktyce klinicznej - przegląd literatury. Ortopedia, Traumatologia, Rehabilitacja. 2018. Vol. 20, no. 5, p. 347–359. DOI 10.5604/01.3001.0012.7281.
[13] McCloskey E, Oden A, Harvey NC, et al. A Meta-Analysis of Trabecular Bone Score in Fracture Risk Prediction and Its Relationship to FRAX. JBMR 2016; 31(5): 940-8
[14] Shoback D, Rosen CJ, Black DM, Cheung AM, Murad MH, Eastell R. Pharmacological Management of Osteoporosis in Postmenopausal Women: An Endocrine Society Guideline Update. J Clin Endocrinol Metab. 2020 Mar 1;105(3):dgaa048. doi: 10.1210/clinem/dgaa048. PMID: 32068863.